암모니아의 합성
인류 문명의 발전에 기여한 화학반응 중 중요하게 다뤄지는 암모니아(Ammonia, NH3)의 합성 반응은 하버-보슈가 개발하였습니다. (Haber-Bosch process) 질소 비료의 원료가 되는 암모니아를 상업적으로 대량 양산하게 됨으로써 식량 문제 해결에 크게 기여한 반응인데요, 고온 고압 조건에서 Fe3O4 촉매를 이용해 공기 중의 질소(N2)와 수소(O2)를 반응시킵니다. 반응식은 단순하죠. 아래와 같습니다.
N2(g) + 3H2(g) → 2NH3(g)
사실 물리화학적으로 이 반응을 진행시키기 위해 설명할 내용들은 많습니다만, 우선 이 단순하면서도 중요한 반응의 양적 관계에 대해 정리를 해보겠습니다. (stochiometry)
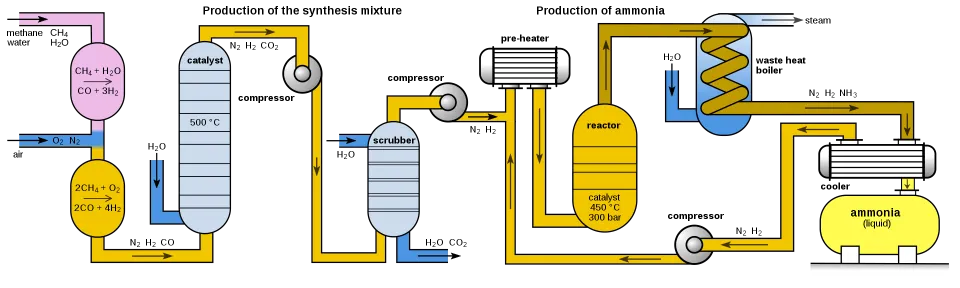
암모니아 합성 반응식의 양적 관계
화학 반응식에서 반응물과 생성물의 종류뿐만 아니라, 물질의 양(mol), 분자 수와 질량, 부피 등의 양적 관계를 확인할 수 있는데요, 계수비와 몰비, 그리고 분자 수비와 부피비가 모두 같기 때문입니다. 여기서 질량비는 계수비와 기본적으로 일치하지 않는다는 점은 기억을 해야 하고요, 암모니아 합성 반응식의 양적 관계를 도표로 정리를 해보면 아래와 같습니다.
| 화학 반응식 | N2(g) | 3H2(g) | 2NH3(g) |
| 물질의 양 (mol) | 1 | 3 | 2 |
| 분자 수 (개) | 6.02 x 10^23 | 3 x 6.02 x 10^23 | 2 x 6.02 x 10^23 |
| 분자 수비 | 1 | 3 | 2 |
| 기체의 부피 (L, 0℃, 1atm) | 1 x 22.4 | 3 x 22.4 | 2 x 22.4 |
| 질량 (g) | 28 | 6 | 34 |
| 질량비 | 14 | 3 | 17 |
1몰(mol)에는 아보가드로수(Avogadro constant)인 6.02 x 10^23개의 입자가 있다는 것, 0℃, 1기압(atm)에서 모든 기체 1몰의 부피는 22.4l로 일정하다는 것도 함께 알고 있어야하겠죠. 위와 같이 화학반응식의 계수비를 통해 양적 관계가 손쉽게 정리가 됩니다.
여기서, 한가지 주의가 필요한 부분은 분자의 부피비는 기체 상태일 때로 한정을 해야 한다는 것입니다. 물질의 상태를 보아야 한다는 것인데요, 예를 들어서 수소와 산소가 반응하여 물을 생성하는 화학반응식에서 분자의 몰비와 분자의 개수비는 2:1:2가 되나 0℃, 1기압에서 분자의 부피비는 2:1:2가 되지 않습니다. 물은 액상으로 존재하기 때문이고, 이 부피비가 성립이 되려면 수증기 상태(H2O(g))여야 가능합니다. 하지만, 해당 온도와 기압에서 수증기 상태가 될 수는 없죠.
2H2(g) + O2(g) → 2H2O(l)
만약 어떠한 문제에서 위의 반응식이 주어지고, H2 : O2 : H2O의 비가 2:1:2의 값을 갖는 것을 찾는다면, 몰비와 분자 개수비는 정답이지만 분자의 부피비와 질량비는 정답이 아닙니다.
'과학' 카테고리의 다른 글
| 에탄올 완전연소반응에서 이산화탄소 부피 구하는 법 (0) | 2023.11.13 |
|---|---|
| 탄화수소의 연소 반응식 유도 방법 (미정계수법) (0) | 2023.11.13 |
| 광합성 세포호흡 산화환원 산화수로 설명 (0) | 2023.11.10 |
| 해양 산성화 반응 정리 (0) | 2023.11.10 |
| 일상 생활 속의 중화반응 (Neutralization reaction) (0) | 2023.10.10 |



댓글